1. Grundläggande kunskap (om du vill se den experimentella delen, vänligen överför direkt till den andra delen)
Som en derivatreaktion av konventionell PCR övervakar realtids-PCR huvudsakligen förändringen av mängden amplifieringsprodukt i varje cykel av PCR-amplifieringsreaktionen i realtid genom förändringen av fluorescenssignalen, och analyserar startmallen kvantitativt genom förhållandet mellan ct-värdet och standardkurvan.
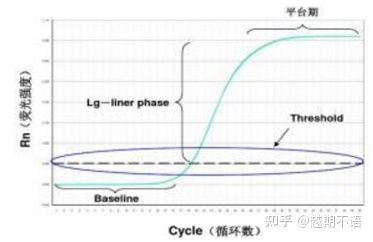
De specifika data för RT-PCR ärbaslinje, fluorescens tröskelochCt-värde.
| baslinje: | Fluorescensvärdet för den 3:e-15:e cykeln är baslinjen (baslinjen), som orsakas av enstaka fel i mätningen. |
| Tröskel (tröskel): | Avser fluorescensdetektionsgränsen inställd på en lämplig position i den exponentiella tillväxtregionen av amplifieringskurvan, vanligtvis 10 gånger standardavvikelsen för baslinjen. |
| CT-värde: | Det är antalet PCR-cykler när fluorescensvärdet i varje reaktionsrör når tröskeln. Ct-värdet är omvänt proportionellt mot mängden initial mall. |
Vanliga märkningsmetoder för RT-PCR:
| metod | fördel | brist | tillämpningsområde |
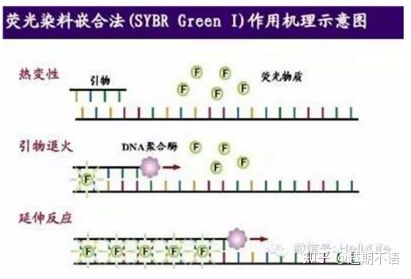
| SYBR GrönⅠ | Bred användbarhet, känslig, billig och bekväm | Primerkraven är höga, benägna att använda ospecifika band | Den är lämplig för kvantitativ analys av olika målgener, forskning om genuttryck och forskning på transgena rekombinanta djur och växter. |
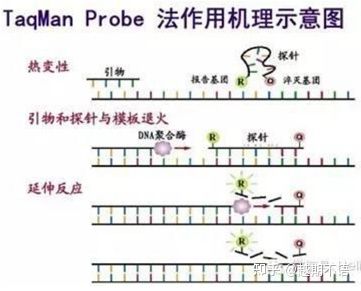
| TaqMan | Bra specificitet och hög repeterbarhet | Priset är högt och lämpar sig endast för specifika mål. | Patogendetektering, läkemedelsresistens genforskning, bedömning av läkemedelseffekt, diagnos av genetiska sjukdomar. |
| molekylär ledstjärna | Hög specificitet, fluorescens, låg bakgrund | Priset är högt, det är bara lämpligt för ett specifikt ändamål, designen är svår och priset är högt. | Specifik genanalys, SNP-analys |
2. Experimentella steg
2.1 Om den experimentella grupperingen- Det måste finnas flera brunnar i gruppen, och det måste finnas biologiska upprepningar.
| ① | Tom kontroll | Används för att upptäcka celltillväxtstatus i experiment |
| ② | Negativ kontroll siRNA (icke-specifik siRNA-sekvens) | Demonstrera specificiteten hos RNAi-verkan.siRNA kan inducera ospecifik stressrespons vid en koncentration av 200nM. |
| ③ | Transfektionsreagenskontroll | Uteslut toxiciteten hos transfektionsreagenset till cellerna eller effekten på uttrycket av målgenen |
| ④ | siRNA mot målgenen | Slå ner uttrycket av målgenen |
| ⑤ (valfritt) | positivt siRNA | Används för att felsöka experimentella system- och driftsproblem |
| ⑥ (valfritt) | Fluorescerande kontroll siRNA | Effektiviteten av celltransfektion kan observeras med ett mikroskop |
2.2 Principer för primerdesign
| Amplifierad fragmentstorlek | Helst vid 100-150bp |
| Primer Längd | 18-25 bp |
| GC-innehåll | 30%-70%, företrädesvis 45%-55% |
| Tm-värde | 58-60 ℃ |
| Sekvens | Undvik T/C kontinuerlig;A/G kontinuerlig |
| 3 slutsekvens | Undvik GC-rik eller AT-rik;den terminala basen är företrädesvis G eller C;det är bäst att undvika T |
| Komplementaritet | Undvik komplementära sekvenser med mer än 3 baser inom primern eller mellan två primers |
| Specificitet | Använd blast-sökning för att bekräfta primerspecificitet |
①SiRNA är artspecifik, och sekvenserna för olika arter kommer att vara olika.
②SiRNA är förpackat i frystorkat pulver, som kan förvaras stabilt i 2-4 veckor i rumstemperatur.
2.3 Verktyg eller reagens som måste förberedas i förväg
| Primer (intern referens) | Inklusive två framåt och bakåt |
| Primers (målgen) | Inklusive två framåt och bakåt |
| Mål-Si-RNA (3 remsor) | I allmänhet kommer företaget att syntetisera 3 remsor och sedan välja en av de tre med RT-PCR |
| Transfektionssats | Lipo2000 osv. |
| RNA Rapid Extraction Kit | För RNA-extraktion efter transfektion |
| Rapid Reverse Transcription Kit | för cDNA-syntes |
| PCR-förstärkningskit | 2×Super SYBR Grön qPCR Master Mix |
2.4 Angående de frågor som måste uppmärksammas i de specifika experimentstegen:
①siRNA-transfektionsprocess
1. För plätering kan du välja 24-brunnars platta, 12-brunnars platta eller 6-brunnars platta (den genomsnittliga RNA-koncentrationen som föreslås i varje brunn i en 24-brunnars platta är cirka 100-300 ng/uL), och den optimala transfektionsdensiteten för celler är upp till 60 %-80 % eller så
2. Transfektionsstegen och specifika krav är strikt i enlighet med instruktionerna.
3. Efter transfektion kan prover samlas in inom 24-72 timmar för mRNA-detektion (RT-PCR) eller proteindetektion inom 48-96 timmar (WB)
② RNA-extraktionsprocess
1. Förhindra kontaminering av exogena enzymer.Det inkluderar främst att bära masker och handskar strikt;använda steriliserade pipettspetsar och EP-rör;vattnet som används i experimentet måste vara RNase-fritt.
2. Det rekommenderas att göra två gånger som föreslagits i snabbextraktionssatsen, vilket verkligen kommer att förbättra renheten och utbytet.
3. Avfallsvätskan får inte vidröra RNA-kolonnen.
③ RNA kvantifiering
Efter att RNA:t har extraherats kan det kvantifieras direkt med Nanodrop , och den lägsta avläsningen kan vara så låg som 10 ng/ul.
④Omvänd transkriptionsprocess
1. På grund av den höga känsligheten hos RT-qPCR bör minst 3 parallella brunnar göras för varje prov för att förhindra att efterföljande Ct blir för olika eller att SD blir för stort för statistisk analys.
2. Frys och tina inte Master mix upprepade gånger.
3. Varje rör/hål måste bytas ut mot en ny spets!Använd inte kontinuerligt samma pipettspets för att lägga till prover!
4. Filmen som fästs på 96-brunnars plattan efter tillsats av provet måste jämnas ut med en platta.Det är bäst att centrifugera innan du sätter den på maskinen, så att vätskan på rörväggen kan rinna ner och ta bort luftbubblor.
⑤ Gemensam kurvanalys
| Ingen period av logaritmisk tillväxt | Möjligen hög koncentration av mall |
| Inget CT-värde | Felaktiga steg för att detektera fluorescerande signaler; nedbrytning av primers eller prober – dess integritet kan detekteras genom PAGE-elektrofores; otillräcklig mängd mall; nedbrytning av mallar – undvika införande av föroreningar och upprepad frysning och upptining i provberedningen; |
| Ct>38 | Låg förstärkningseffektivitet;PCR-produkten är för lång;olika reaktionskomponenter bryts ned |
| Linjär förstärkningskurva | Prober kan delvis brytas ned genom upprepade frys-upptiningscykler eller långvarig exponering för ljus |
| Skillnaden i dubbla hål är särskilt stor | Reaktionslösningen är inte fullständigt smält eller reaktionslösningen är inte blandad;PCR-instrumentets termiska bad är förorenat av fluorescerande ämnen |
2.5 Om dataanalys
Dataanalysen av qPCR kan delas in i relativ kvantifiering och absolut kvantifiering.Till exempel, celler i behandlingsgruppen jämfört med celler i kontrollgruppen,
Hur många gånger X-genens mRNA förändras, detta är relativ kvantifiering;i ett visst antal celler, X-genens mRNA
Hur många exemplar det finns, detta är absolut kvantifiering.Vanligtvis är det vi använder mest i laboratoriet den relativa kvantitativa metoden.Vanligtvis,2-ΔΔct-metodenanvänds mest i experiment , så endast denna metod kommer att introduceras i detalj här.
2-ΔΔct-metod: Det erhållna resultatet är skillnaden i uttrycket av målgenen i experimentgruppen i förhållande till målgenen i kontrollgruppen.Det krävs att amplifieringseffektiviteten för både målgenen och den interna referensgenen är nära 100 %, och den relativa avvikelsen bör inte överstiga 5 %.
Beräkningsmetoden är följande:
Δct-kontrollgrupp = ct-värde för målgen i kontrollgrupp – ct-värde för intern referensgen i kontrollgrupp
Δct experimentell grupp = ct-värde för målgenen i experimentgruppen – ct-värde för den interna referensgenen i experimentgruppen
ΔΔct=Δct experimentell grupp-Δct kontrollgrupp
Beräkna slutligen multipeln av skillnaden i uttrycksnivå:
Change Fold=2-ΔΔct (motsvarande excel-funktionen är POWER)
Relaterade produkter:
Posttid: 20 maj 2023